海外メディアTech Xploreによると、MITの研究者らは最近、新しいタンパク質分子の構造を事前に予測し、医薬品開発の効率を向上させることができる「EquBind」と呼ばれる新しいモデルを開発したとのこと。
現在、この技術は業界に認知されており、この技術を解説した論文は7月に開催される機械学習国際会議(ICML)にも採択される予定です。
1. 速度が 1200 倍に向上し、EquBind モデルは薬物のような分子を迅速にスクリーニングできます
現在、薬物の研究開発は時間と費用がかかる問題です。その主な理由は、医薬品の開発に非常に費用がかかることです。このコストには、数十億ドルの設備投資だけでなく、数十年に及ぶ研究時間も含まれます。
そして、研究開発の過程では、90% の医薬品は効果がなかったり副作用が多すぎたりするために失敗し、食品医薬品局の検査に合格して販売が承認されるのは 10% のみです。
したがって、製薬会社は、開発に成功した薬の価格を引き上げて、薬の失敗による損失を補填するため、現在、一部の薬の価格は高止まりしています。

▲タンパク質の分子構造の一部
研究者が薬を開発したい場合は、まず開発の可能性を持つ薬のような分子を見つけなければなりません。医薬品開発の進展が遅いもう一つの重要な理由は、膨大な数の既存の医薬品のような分子です。現在、ドラッグライク分子は1,016種類も存在するというデータがあり、これは既存の分子計算モデルの計算上限をはるかに超えています。
このような大きな分子をデータで処理し、医薬品開発のプロセスをスピードアップするために、マサチューセッツ工科大学電気工学およびコンピューターサイエンス学科の大学院 1 年生である Hannes St rk は、幾何学的な深層構造を開発しました。 「EquBind」と呼ばれる学習モデル。 EquBind は、既存の最速の分子計算ドッキング モデルよりも 1,200 倍速く実行され、薬物のような分子をより速く見つけることができます。
2. EquBind モデルはタンパク質構造を正確に予測し、医薬品開発の効率を向上させることができます
現在、ほとんどの従来の分子コンピューティング ドッキング モデルは、「リガンド-タンパク質」(リガンド-タンパク質) と呼ばれる方法を使用しています。 -タンパク質結合) 薬物様分子を検索する方法。具体的には、モデルはまず多数のサンプル分子を受け取り、次にリガンドをさまざまな分子に結合させ、次にモデルがさまざまな分子をスコアリングし、最終的なランキングを使用して最適な分子を選択する必要があります。ただし、このアプローチには複雑なプロセスがあり、モデルは薬物のような分子を見つける効率が低くなります。
Hannes St rk は、このプロセスを鮮やかな比喩で表現し、次のように述べています:「これまでの典型的な 'リガンド-タンパク質' アプローチは、モデルに鍵穴の多い錠前に鍵を挿入させようとするようなものでした。モデルは鍵と各鍵穴の間の適合性をスコアリングし、最も適切なものを選択することに多くの時間を費やしています。」
彼はさらに説明しました: 「そして、EquBind は最も時間のかかるステップをスキップできます。 、予測することができます。」新しい分子に遭遇したときに、事前に最も適切な「鍵穴」を見つけることを「ブラインドドッキング」と呼びます。EquBind には、モデルが分子の基本構造を学習するのに役立つ幾何学的推論アルゴリズムが組み込まれています。このアルゴリズムにより、EquBind は直接新しい分子に遭遇したときに、さまざまな位置を試して採点することに多くの時間を費やすことなく、最適な位置を予測できます。」

▲マサチューセッツ工科大学
3. EquBind モデルは業界でうまく使用されており、著者はさらなるフィードバックを楽しみにしています
このモデルは、治療会社 Relay の最高データ責任者である Pat Walters の注目を集めました。ウォルスター氏は、ハンネス・シュテルク氏の研究グループがこのモデルを肺がん、白血病、胃腸腫瘍の治療薬の開発に使用することを提案した。一般に、これらの分野の医薬品に使用されるタンパク質リガンドは、従来の方法のほとんどを使用してドッキングするのは困難ですが、EquBind はそれらを正常にドッキングできます。

▲肺がん治療のための 2 つの阻害薬
Walters 氏は次のように述べています。「EquBind は、タンパク質のドッキング問題に対する独自の解決策を提供します。構造などの問題を解決します。」 「予測と結合部位の同定。この方法は、何千もの公開された結晶構造情報を有効に活用でき、EquBind は新しい方法でこの分野に影響を与える可能性があります。」
投稿 この技術に関する論文は、国際学術誌に受理される予定です。 7 月に開催される機械学習カンファレンス (ICML) 論文の著者であるハンネス・ストルク氏は、「このカンファレンスで EquBind モデルを改善するための提案を受け取ることを楽しみにしています。」
結論: 互換性AI と医薬品の連携は優れており、開発の勢いは絶好調です
AI 医薬品は、2020 年に世間の注目を集めたばかりの新興分野です。
製薬分野は自然な AI シナリオです。新薬の研究開発はサイクルが長く、コストが高く、成功率が低いため、AI の余地が大きく残されています。機械は独自にデータを学習し、データをマイニングし、専門家の経験を超えて医薬品の研究開発ルールを要約し、医薬品の研究と開発を最適化できます。これにより、あらゆる面で医薬品の研究開発の効率と成功率が向上するだけでなく、研究開発費や試行錯誤コストの削減も期待されます。
このような特徴と開発の可能性により、現在AI医薬品は勢いを増しています。しかし、業界関係者の中には「AIは製薬プロセスにおける補助的な役割にすぎず、業界固有のプロセスや仕組みを回避することはできない。10年分の仕事を2~3年で終わらせるのは不可能だ」と悲観的な見方もある。
しかし全体として、AI医薬品の分野では依然として新たな技術的進歩があり、開発は急成長しています。
以上が効率1200倍アップ! MIT が新しい AI 製薬モデルを開発の詳細内容です。詳細については、PHP 中国語 Web サイトの他の関連記事を参照してください。
 AIインデックス2025を読む:AIはあなたの友人、敵、または副操縦士ですか?Apr 11, 2025 pm 12:13 PM
AIインデックス2025を読む:AIはあなたの友人、敵、または副操縦士ですか?Apr 11, 2025 pm 12:13 PMスタンフォード大学ヒト指向の人工知能研究所によってリリースされた2025年の人工知能インデックスレポートは、進行中の人工知能革命の良い概要を提供します。 4つの単純な概念で解釈しましょう:認知(何が起こっているのかを理解する)、感謝(利益を見る)、受け入れ(顔の課題)、責任(責任を見つける)。 認知:人工知能はどこにでもあり、急速に発展しています 私たちは、人工知能がどれほど速く発展し、広がっているかを強く認識する必要があります。人工知能システムは絶えず改善されており、数学と複雑な思考テストで優れた結果を達成しており、わずか1年前にこれらのテストで惨めに失敗しました。 2023年以来、複雑なコーディングの問題や大学院レベルの科学的問題を解決することを想像してみてください
 Meta Llama 3.2を始めましょう - 分析VidhyaApr 11, 2025 pm 12:04 PM
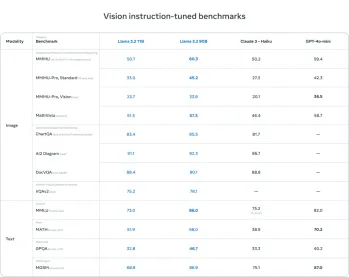
Meta Llama 3.2を始めましょう - 分析VidhyaApr 11, 2025 pm 12:04 PMメタのラマ3.2:マルチモーダルとモバイルAIの前進 メタは最近、ラマ3.2を発表しました。これは、モバイルデバイス向けに最適化された強力なビジョン機能と軽量テキストモデルを特徴とするAIの大幅な進歩です。 成功に基づいてo
 AVバイト:Meta' s llama 3.2、GoogleのGemini 1.5などApr 11, 2025 pm 12:01 PM
AVバイト:Meta' s llama 3.2、GoogleのGemini 1.5などApr 11, 2025 pm 12:01 PM今週のAIの風景:進歩、倫理的考慮、規制の議論の旋風。 Openai、Google、Meta、Microsoftのような主要なプレーヤーは、画期的な新しいモデルからLEの重要な変化まで、アップデートの急流を解き放ちました
 マシンと話すための人的費用:チャットボットは本当に気にすることができますか?Apr 11, 2025 pm 12:00 PM
マシンと話すための人的費用:チャットボットは本当に気にすることができますか?Apr 11, 2025 pm 12:00 PMつながりの慰めの幻想:私たちはAIとの関係において本当に繁栄していますか? この質問は、MIT Media Labの「AI(AHA)で人間を進める」シンポジウムの楽観的なトーンに挑戦しました。イベントではCondedgを紹介している間
 PythonのScipy Libraryの理解Apr 11, 2025 am 11:57 AM
PythonのScipy Libraryの理解Apr 11, 2025 am 11:57 AM導入 あなたが科学者またはエンジニアで複雑な問題に取り組んでいると想像してください - 微分方程式、最適化の課題、またはフーリエ分析。 Pythonの使いやすさとグラフィックスの機能は魅力的ですが、これらのタスクは強力なツールを必要とします
 ラマ3.2を実行する3つの方法-Analytics VidhyaApr 11, 2025 am 11:56 AM
ラマ3.2を実行する3つの方法-Analytics VidhyaApr 11, 2025 am 11:56 AMメタのラマ3.2:マルチモーダルAIパワーハウス Metaの最新のマルチモーダルモデルであるLlama 3.2は、AIの大幅な進歩を表しており、言語理解の向上、精度の向上、および優れたテキスト生成機能を誇っています。 その能力t
 Dagsterでデータ品質チェックを自動化しますApr 11, 2025 am 11:44 AM
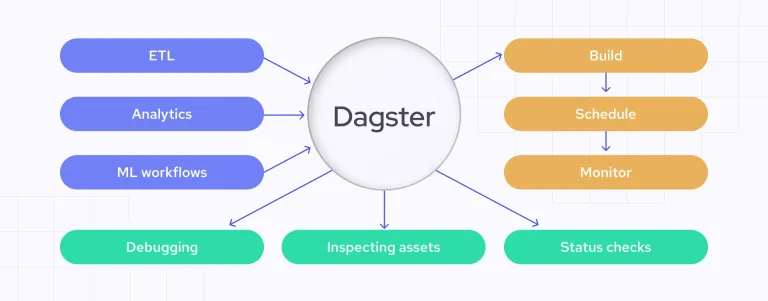
Dagsterでデータ品質チェックを自動化しますApr 11, 2025 am 11:44 AMデータ品質保証:ダグスターと大きな期待でチェックを自動化する データ駆動型のビジネスにとって、高いデータ品質を維持することが重要です。 データの量とソースが増加するにつれて、手動の品質管理は非効率的でエラーが発生しやすくなります。
 メインフレームはAI時代に役割を果たしていますか?Apr 11, 2025 am 11:42 AM
メインフレームはAI時代に役割を果たしていますか?Apr 11, 2025 am 11:42 AMMainFrames:AI革命のUnsung Heroes サーバーは汎用アプリケーションで優れており、複数のクライアントの処理を行いますが、メインフレームは大量のミッションクリティカルなタスク用に構築されています。 これらの強力なシステムは、頻繁にヘビルで見られます


ホットAIツール
Undresser.AI Undress
リアルなヌード写真を作成する AI 搭載アプリ
AI Clothes Remover
写真から衣服を削除するオンライン AI ツール。

Undress AI Tool
脱衣画像を無料で

Clothoff.io
AI衣類リムーバー

AI Hentai Generator
AIヘンタイを無料で生成します。

人気の記事

ホットツール

ゼンドスタジオ 13.0.1
強力な PHP 統合開発環境

MinGW - Minimalist GNU for Windows
このプロジェクトは osdn.net/projects/mingw に移行中です。引き続きそこでフォローしていただけます。 MinGW: GNU Compiler Collection (GCC) のネイティブ Windows ポートであり、ネイティブ Windows アプリケーションを構築するための自由に配布可能なインポート ライブラリとヘッダー ファイルであり、C99 機能をサポートする MSVC ランタイムの拡張機能が含まれています。すべての MinGW ソフトウェアは 64 ビット Windows プラットフォームで実行できます。

mPDF
mPDF は、UTF-8 でエンコードされた HTML から PDF ファイルを生成できる PHP ライブラリです。オリジナルの作者である Ian Back は、Web サイトから「オンザフライ」で PDF ファイルを出力し、さまざまな言語を処理するために mPDF を作成しました。 HTML2FPDF などのオリジナルのスクリプトよりも遅く、Unicode フォントを使用すると生成されるファイルが大きくなりますが、CSS スタイルなどをサポートし、多くの機能強化が施されています。 RTL (アラビア語とヘブライ語) や CJK (中国語、日本語、韓国語) を含むほぼすべての言語をサポートします。ネストされたブロックレベル要素 (P、DIV など) をサポートします。

ドリームウィーバー CS6
ビジュアル Web 開発ツール

SublimeText3 Mac版
神レベルのコード編集ソフト(SublimeText3)







