효율성이 1200배 증가했습니다! MIT, 새로운 AI 제약 모델 개발
- 王林앞으로
- 2023-04-09 18:31:011422검색
외신 Tech Xplore에 따르면, MIT 연구진은 최근 새로운 단백질 분자의 구조를 미리 예측하고 신약 개발의 효율성을 높일 수 있는 EquBind라는 새로운 모델을 개발했다고 합니다.
현재 이 기술은 업계에서 인정을 받았으며, 이 기술을 기술한 논문은 7월 ICML(International Conference on Machine Learning)에서도 채택될 예정입니다.
1. 속도는 1200배 증가하고 EquBind 모델은 약물 유사 분자를 빠르게 스크리닝할 수 있습니다
현재 약물 연구 및 개발은 길고 비용이 많이 드는 과정입니다. 주된 이유는 약물 개발 비용이 매우 비싸기 때문입니다. 이 비용에는 수십억 달러의 자본 투자뿐만 아니라 수십 년의 연구 시간도 포함됩니다.
그리고 연구 개발 과정에서 약품의 90%는 효과가 없거나 너무 많은 부작용으로 인해 실패하게 됩니다. 단 10%의 약품만이 식품의약청 검사를 통과하고 시판 승인을 받을 수 있습니다.
따라서 제약회사들은 실패한 약품으로 인한 손실을 만회하기 위해 성공적으로 개발된 약품의 가격을 인상할 예정이어서 현재 일부 약품의 가격이 여전히 높은 상태입니다.
▲일부 단백질 분자 구조
연구원이 약물을 개발하려면 먼저 개발 가능성이 있는 약물과 유사한 분자를 찾아야 합니다. 약물 개발이 느리게 진행되는 또 다른 중요한 이유는 기존 약물과 유사한 분자가 엄청나게 많기 때문입니다. 데이터에 따르면 현재 기존의 약물 유사 분자는 1,016개에 달하며, 이는 기존 분자 계산 모델의 계산 상한을 훨씬 초과하는 숫자입니다.
이렇게 방대한 데이터가 담긴 분자를 처리하고 신약 개발 속도를 높이기 위해 MIT 전자공학 및 컴퓨터공학과 1학년 대학원생 Hannes Strk는 ""라는 기하학적 딥러닝 모델을 개발했습니다. 에쿠바인드". EquBind는 기존의 가장 빠른 분자 계산 도킹 모델보다 1,200배 더 빠르게 실행되므로 약물과 유사한 분자를 더 빠르게 찾을 수 있습니다.
2. EquBind 모델은 단백질 구조를 정확하게 예측하고 약물 개발 효율성을 향상시킬 수 있습니다.
현재 대부분의 전통적인 분자 컴퓨팅 도킹 모델은 "리간드-단백질 결합" 약물 유사 분자라는 방법을 통해 발견됩니다. 구체적으로, 모델은 먼저 많은 수의 샘플 분자를 수신한 다음 리간드가 다양한 분자에 결합되도록 한 다음 모델이 다양한 분자에 점수를 매긴 다음 최종 순위를 사용하여 가장 적합한 분자를 선택해야 합니다. 그러나 이 접근 방식은 프로세스가 복잡하고 모델이 약물 유사 분자를 찾는 데 효율성이 떨어집니다.
Hannes St rk는 이 과정을 생생하게 비유했습니다. "이전의 전형적인 '리간드-단백질' 접근 방식은 모델이 열쇠 구멍이 많은 자물쇠에 열쇠를 삽입하도록 하는 것과 같았습니다. 모델은 많은 시간을 소비했습니다. 시간을 이용해 열쇠와 각 열쇠 구멍 사이의 적합도를 계산한 다음 가장 적합한 것을 선택하세요." 사전에 적합한 '열쇠구멍'을 '블라인드 도킹'이라고 합니다. EquBind에는 모델이 분자의 기본 구조를 학습하는 데 도움이 되는 기하학적 추론 알고리즘이 내장되어 있어 EquBind가 가장 적합한 위치를 찾을 수 있습니다. 많은 시간을 들여 다양한 위치를 시도하고 채점하지 않고도 분자 시점에서 직접 예측할 수 있습니다.”
 ▲MIT
▲MIT
3. EquBind 모델은 업계에서 성공적으로 사용되었으며 저자는 더 많은 것을 기대합니다. . 피드백
이 모델은 치료 회사 Relay의 최고 데이터 책임자인 Pat Walters의 관심을 끌었습니다. Walster는 Hannes Störk의 연구 그룹이 이 모델을 사용하여 폐암, 백혈병 및 위장 종양에 대한 약물을 개발할 것을 제안했습니다. 일반적으로 이 분야의 약물에 사용되는 단백질 리간드는 대부분의 전통적인 방법으로는 도킹하기 어렵지만 EquBind는 성공적으로 도킹할 수 있습니다.
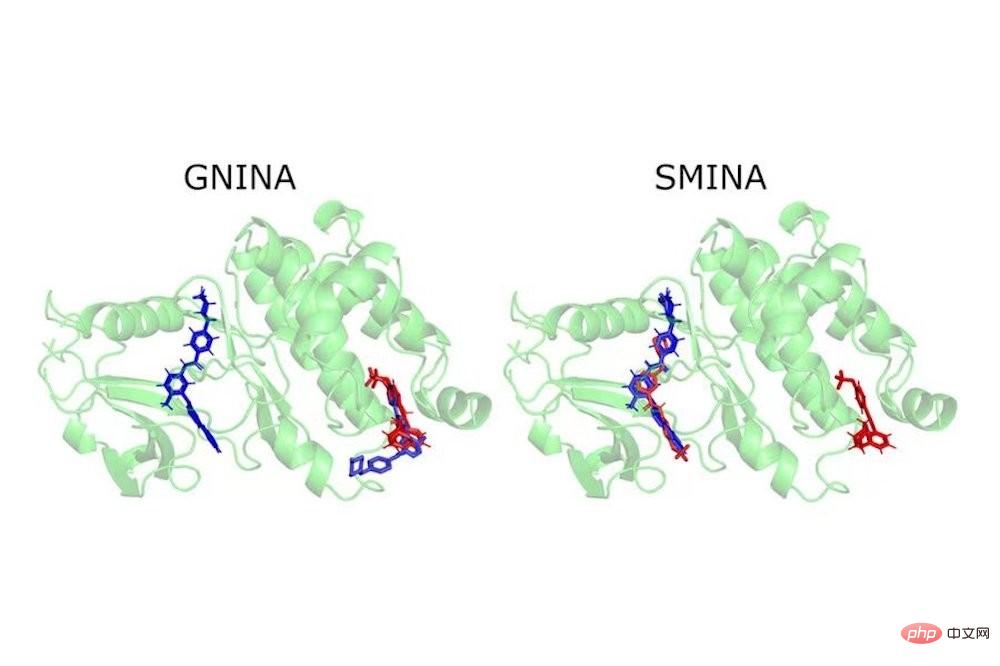 ▲폐암 치료를 위한 두 가지 억제제
▲폐암 치료를 위한 두 가지 억제제
Walters는 "EquBind는 단백질 도킹 문제에 대한 독특한 솔루션을 제공하여 구조 예측 및 결합 부위 식별 문제를 해결합니다. 이 방법은 공개적으로 사용 가능한 수천 개의 결정 구조 정보를 사용하여 EquBind는 새로운 방식으로 해당 분야에 영향을 미칠 수 있습니다."
이 기술을 출판한 논문은 7월 ICML(International Conference on Machine Learning)에서 승인될 예정입니다. Hannes St rk, 저자 논문에서는 "이번 컨퍼런스에서 EquBind 모델 개선을 위한 몇 가지 제안을 기대하고 있습니다."
결론: AI는 의약품과의 호환성이 뛰어나며 개발 모멘텀이 급성장하고 있습니다.
AI Pharmaceuticals는 2020년에야 대중의 관심을 끌었습니다.
제약 분야는 자연스러운 AI 시나리오입니다. 신약 연구 개발의 긴 주기, 높은 비용, 낮은 성공률로 인해 AI가 사용될 여지가 커졌습니다. 기계는 자동으로 데이터를 학습하고, 데이터를 마이닝하고, 전문가 경험을 넘어 약물 연구 및 개발 규칙을 요약한 다음 최적화할 수 있습니다. 이는 모든 측면에서 신약 연구개발의 효율성과 성공률을 향상시킬 수 있을 뿐만 아니라, 연구개발 비용과 시행착오 비용도 절감할 수 있을 것으로 기대됩니다.
이러한 특성과 개발 가능성으로 인해 현재 AI 의약품이 탄력을 받고 있습니다. 그러나 업계 일각에서는 AI가 제약 공정에서 보조 역할만 할 뿐, 업계 고유의 프로세스와 메커니즘을 우회할 수는 없다고 비관적이다.
그러나 전반적으로 AI 의약품 분야에는 여전히 새로운 기술 혁신이 존재하며 개발이 호황을 누리고 있습니다.
위 내용은 효율성이 1200배 증가했습니다! MIT, 새로운 AI 제약 모델 개발의 상세 내용입니다. 자세한 내용은 PHP 중국어 웹사이트의 기타 관련 기사를 참조하세요!

