복주대학교와 Yuanxing 지능형 약물팀의 설명 약물 AI 모델인 DDI를 효율적이고 정확하게 예측하는 방법이 Nature 저널에 게재되었습니다.
- WBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWB원래의
- 2024-09-02 15:13:00415검색

예기치 않은 약물 상호작용(DDI)은 심각한 약물 부작용을 일으킬 가능성이 높기 때문에 약물 연구 및 임상 적용에 있어서 중요한 문제입니다. 반응 또는 약물 금단.
많은 딥러닝 모델이 DDI 예측에서 좋은 결과를 얻었지만, DDI의 근본 원인을 밝히는 모델 해석 가능성은 널리 탐구되지 않았습니다.
푸저우 대학교, 푸젠 의과대학교 제1부속병원 및 Yuanxing 지능형 의학의 연구원들은 과목의 DDI 예측 플롯을 기반으로 학습을 위한 로컬-글로벌 셀프 어텐션 및 공동 관심을 갖춘 딥 러닝 프레임워크인 MeTDDI를 제안했습니다.
해석 가능성과 관련하여 연구자들은 73개 약물(13,786개 DDI)에 대해 광범위한 평가를 수행했으며, MeTDDI는 58개 약물이 포함된 5,602개 DDI의 구조 메커니즘을 정확하게 설명할 수 있습니다. 또한 MeTDDI는 복잡한 DDI 메커니즘을 설명하고 DDI 위험을 줄일 수 있는 잠재력을 보여줍니다.
MeTDDI는 DDI 메커니즘 탐구에 대한 새로운 관점을 제공하여 약물 발견 및 다중약제를 촉진하여 환자에게 보다 안전한 치료법을 제공합니다.
이 연구의 제목은 "로컬-글로벌 셀프 어텐션을 통한 약물-약물 상호 작용 예측을 위한 학습 모티브 기반 그래프"이며 2024년 8월 27일 "Nature Machine Intelligence"에 게재되었습니다.

노화 및 복합상병으로 인해 약물 조합이나 다중약물요법이 널리 사용되고 있으며 이는 공중 보건과 경제에 영향을 미칠 수 있습니다. 다중약제의 치료적 이점에도 불구하고, 의도하지 않은 약물-약물 상호작용(DDI)이 발생할 위험이 있으며, 이는 심각한 약물유해반응(ADR) 또는 심지어 중단으로 이어질 수 있습니다.
따라서 DDI를 미리 예측하면 약물 연구 및 임상 환경에 큰 이점을 가져다 주어 약물 안전성을 향상하고 환자의 건강을 보호할 수 있습니다. 시험관 내 및 생체 내 실험을 통한 DDI 평가는 유용하지만 비용이 많이 들고 시간이 많이 걸리며 힘들기 때문에 대규모 DDI 스크리닝의 실용성을 방해합니다.
오늘날 딥 러닝 모델은 높은 처리량의 정확한 DDI 예측은 물론 근본 원인 설명을 위한 유망한 대안으로 떠올랐습니다.
최근 연구에서 푸저우대학교, 푸젠의과대학교 제1부속병원, 위안싱지능의학 연구팀은 대사 매개 약물 상호 작용(MMDDI) 예측에 중점을 두고 심층 분자 구조 기반 학습을 제안했습니다. MMDDI 예측을 위한 프레임워크 MeTDDI.
이 방법은 주로 DDI 예측의 세 가지 과제를 해결하는 데 사용됩니다. (1) 분자 내 및 분자간 하부 구조 상호 작용 학습, (2) DDI 관련 약물 대사 예측, (3) 모델 해석 가능성을 광범위하게 제공 및 평가합니다.
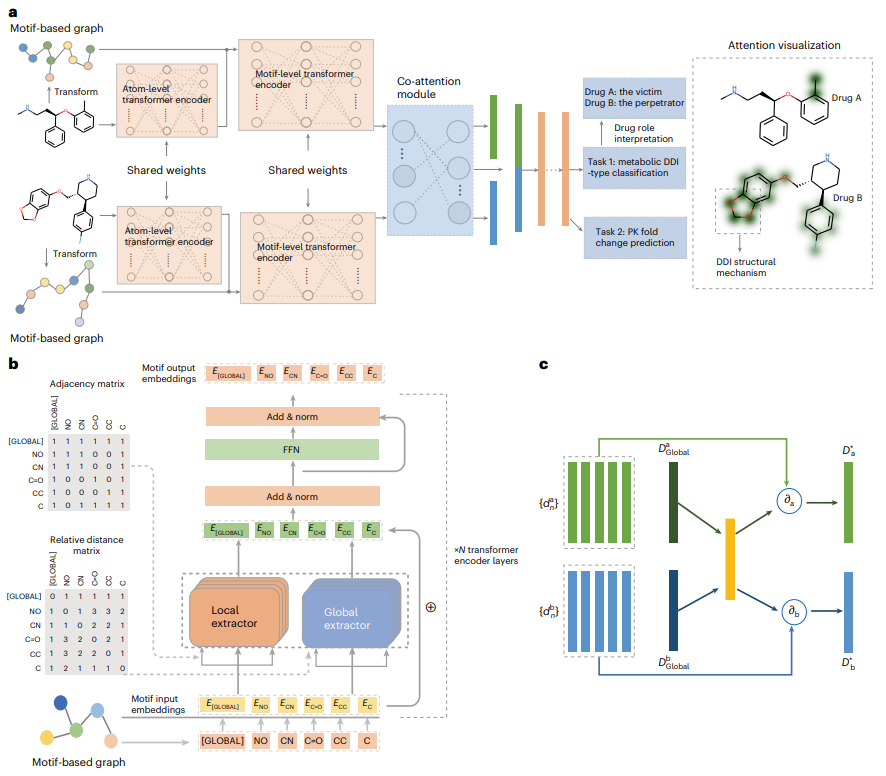
MeTDDI는 로컬-글로벌 셀프 어텐션과 조인트 어텐션 구조의 이점을 활용하여 모티프를 기반으로 그래프 내/간 분자 내 및 분자간 하위 구조 상호 작용을 효과적으로 학습하여 DDI 추론을 수행할 수 있습니다.
평가 결과 분류 및 회귀 작업 모두 기준선 대비 경쟁력 있는 성능을 달성하는 것으로 나타났습니다. MeTDDI는 또한 DDI에서 약물(가해자 또는 피해자)의 기계적 역할을 정확하게 식별하고 가해자가 피해자 PK에 미치는 영향을 정량화할 수 있으며 이는 약물 연구 및 임상 적용 모두에 매우 유용합니다.
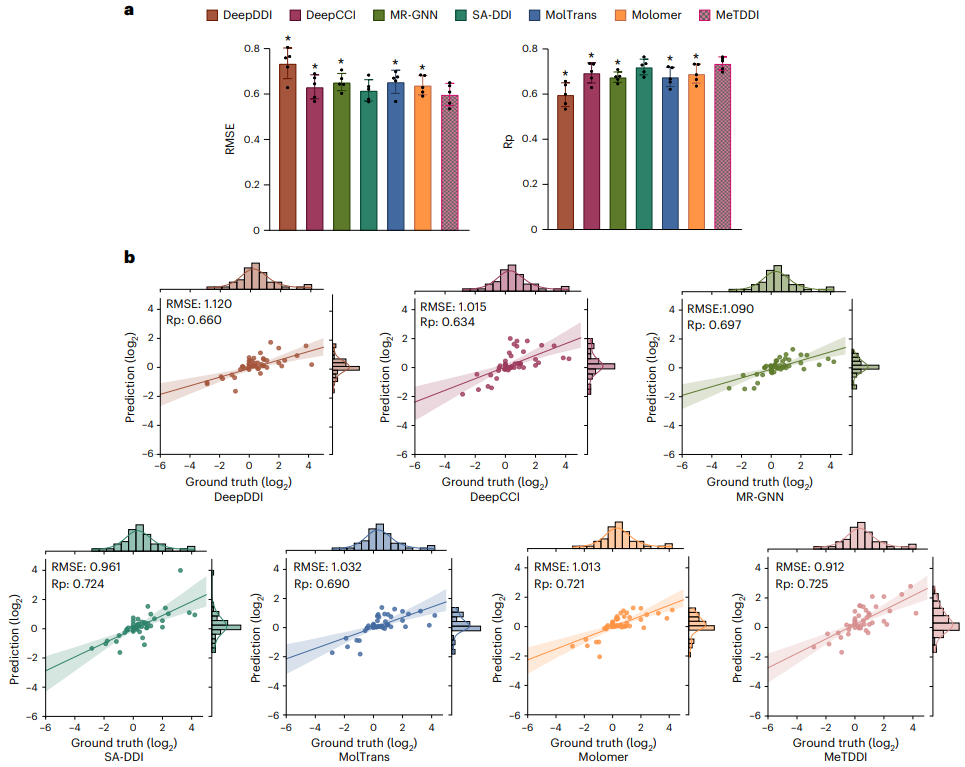
모델 해석 가능성과 관련하여 MeTDDI는 DDI와 관련된 주요 기계적 하위 구조를 식별하는 능력을 보여줍니다.
첫째, MeTDDI로 시각화한 주요 하위 구조는 73개의 대표적인 화합물(13,786개의 DDI 쌍 포함) 분석을 통해 문헌에 보고된 것과 대략 일치합니다.
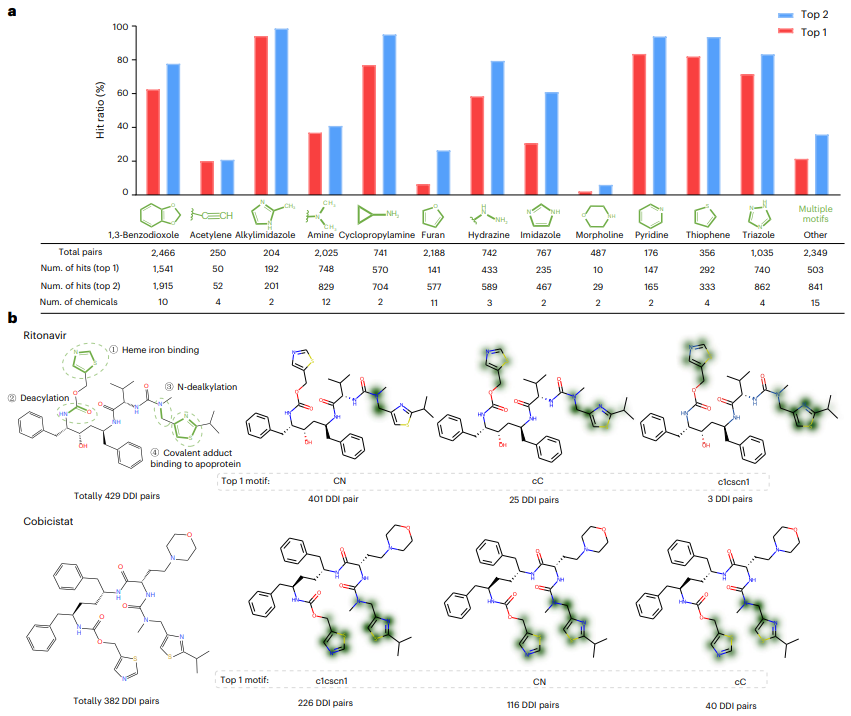
둘째, 연구진은 MeTDDI와 두 가지 최신 모델인 CIGIN과 CGIB의 모델 해석성을 평가했습니다. 결과는 MeTDDI가 모델 해석성 측면에서도 탁월한 성능을 보이는 것을 보여줍니다.
또한 MeTDDI는 효소 억제와 관련된 화학 물질의 대사 부위를 강조할 수 있습니다.
MeTDDI의 장점
전통적인 방법은 피해자를 충분히 고려하지 않고 가해자의 대사효소 억제를 시험관 내에서 테스트하는 방식으로 DDI의 메커니즘을 설명할 뿐입니다. 이는 가해자의 효소 억제 능력이 피해자의 화학적 특성에 따라 달라질 수 있기 때문에 문제가 됩니다.
Das Opfer kann das Bindungs- oder Interaktionsmuster des Täters mit Stoffwechselenzymen (insbesondere CYP) verändern, was zu verschiedenen Enzymhemmmechanismen führt. Dies könnte erklären, warum einige Chemikalien wie Ethinylestradiol und Gestoden, die bei alleiniger Anwendung in vitro starke Inhibitoren von Stoffwechselenzymen darstellen, in Kombination mit ihren Opfern weniger wirksam sind. Dies könnte erklären, warum in der Studie mit Ethinylestradiol, bei dem es sich vermutlich um einen Mechanismus zur Inaktivierung von CYP3A4 in vitro handelt, nur zwei Reaktionen beobachtet wurden.
Darüber hinaus zeigen Fallstudien zu Paroxetin und Itraconazol, dass MeTDDI Motivveränderungen in Chemikalien korrekt vorhersagt und mit Ergebnissen aus biologischen Experimenten übereinstimmt. Dies zeigt sein Potenzial, Forschern dabei zu helfen, die Struktur von Arzneimitteln zu modifizieren, um MMDDI-Risiken zu mindern.
Zusammenfassend lässt sich sagen, dass MeTDDI die DDI-Vorhersagefähigkeiten verbessert und eine neue Perspektive für das Verständnis und die Erforschung von DDI-Mechanismen bietet, was die Arzneimittelentwicklung und Polypharmazie erleichtern und dadurch sicherere Behandlungen für Patienten ermöglichen wird.
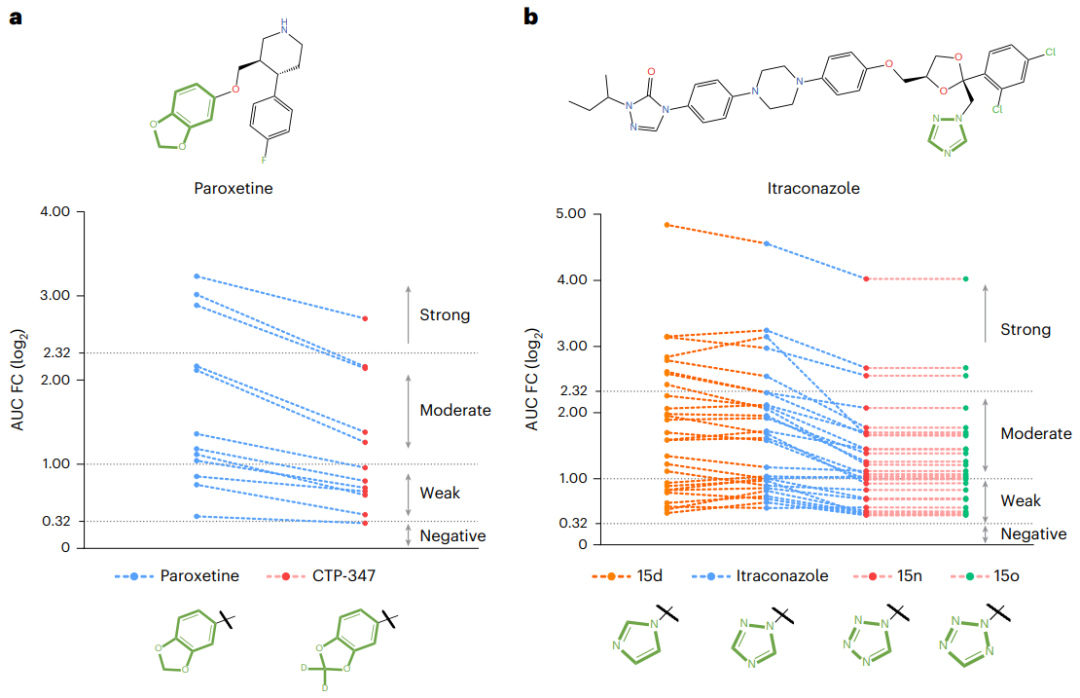
Abbildung: Zwei Fallstudien zur DDI-Minderung mithilfe von MeTDDI. (Quelle: Papier) Verbesserungsrichtungen von MeTDDI
MeTDDI hat viele Vorteile, weist aber gleichzeitig auch einige Einschränkungen auf.
Erstens ist eine genaue Vorhersage in schwierigen Szenarien eine Herausforderung. Dies kann auf die Vielfalt und Komplexität der DDI-Mechanismen und die Einschränkungen zurückzuführen sein, die sich aus der alleinigen Abhängigkeit von der Arzneimittelstruktur ergeben.
Da MMDDI erfordert, dass beide Medikamente an denselben Stoffwechselenzymen interagieren, können Enzymmerkmale zum besseren Lernen in das Modell integriert werden. Einige Stoffwechselenzyme (z. B. CYP) weisen jedoch eine außerordentliche Flexibilität in Bezug auf die Wechselwirkungsstellen zwischen Arzneimitteln und Enzymen auf, weshalb die Modellierung der Enzymeigenschaften weiterhin eine Herausforderung darstellt.
Zweitens basiert der auf MeTDDI trainierte Datensatz auf Arzneimitteletiketten der FDA, bei denen es sich um statistische Beobachtungen der Bevölkerung handelt und die möglicherweise nicht die Merkmale einzelner Patienten widerspiegeln. Daher sollten, sofern verfügbar, individuelle Patientendaten berücksichtigt werden, um Modelle zu entwickeln und in Zukunft genauere Vorhersagen zu treffen. Drittens kann MeTDDI Schwierigkeiten haben, Wechselwirkungen von mehr als zwei Arzneimitteln gleichzeitig vorherzusagen.
Eine allgemeine Praxis zur Gewährleistung der Polypharmazie besteht jedoch darin, nach paarweisen DDIs zwischen allen möglichen Arzneimittelpaaren zu suchen. MeTDDI kann direkt zur Vorhersage von DDIs zwischen mehreren Arzneimitteln eingesetzt werden, indem alle Arzneimittelpaare aufgelistet werden.
Schließlich können für neu entdeckte Unterstrukturen, die DDI zugrunde liegen, alternative Techniken wie molekulares Docking als ergänzende Ansätze eingesetzt werden, um die Glaubwürdigkeit der MeTDDI-Visualisierungsfähigkeiten zu erhöhen. Und die Forscher sagen, dass molekulares Docking ein wertvolles ergänzendes Werkzeug zu MeTDDI ist.
Link zum Papier: https://www.nature.com/articles/s42256-024-00888-6
위 내용은 복주대학교와 Yuanxing 지능형 약물팀의 설명 약물 AI 모델인 DDI를 효율적이고 정확하게 예측하는 방법이 Nature 저널에 게재되었습니다.의 상세 내용입니다. 자세한 내용은 PHP 중국어 웹사이트의 기타 관련 기사를 참조하세요!

