Heim >Technologie-Peripheriegeräte >KI >Durchbruch in der RNA-Arzneimittelentwicklung: Das erste RNA-Basismodell enthüllt Messtechnik auf der Ebene von mehr als einer Milliarde Nukleotiden
Durchbruch in der RNA-Arzneimittelentwicklung: Das erste RNA-Basismodell enthüllt Messtechnik auf der Ebene von mehr als einer Milliarde Nukleotiden
- WBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBOYWBnach vorne
- 2023-12-28 09:29:251110Durchsuche
Herausgeber |. KX
Kürzlich gab das Biotechnologieunternehmen Atomic AI die erfolgreiche Entwicklung des ersten groß angelegten Sprachmodells (LLM) bekannt, das chemische Kartierungsdaten nutzt. Atomic AI kombiniert fortschrittliche Techniken des maschinellen Lernens mit der neuesten Strukturbiologie, um die Geheimnisse der RNA-Wirkstoffentdeckung zu lösen
Forscher von Atomic AI haben eine neue Plattformkomponente entwickelt, die die firmeninterne, maßgeschneiderte Nasslaboranalyse-Sammlung umfangreicher chemischer Kartierungsdaten nutzt. Die Wissenschaftler sammelten Daten von Millionen von RNA-Sequenzen und führten mehr als eine Milliarde Messungen auf Nukleotidebene durch. Basierend auf diesen Daten entwickelt ATOM-1 ein umfassendes Verständnis der RNA, das dann zur Optimierung der Eigenschaften verschiedener RNA-Muster genutzt werden kann.
Atomic AI veröffentlichte am 14. Dezember einen Artikel mit dem Titel „ATOM-1: RNA konstruiert basierend auf chemischen Kartendaten. Ein Preprint-Papier“ Basic Model of Structure and Function“, das auf bioRxiv veröffentlicht wurde. In diesem Artikel beschreibt Atomic AI ausführlich seine einzigartigen ATOM-1™-Plattformkomponenten. Dieses Grundmodell kann die Struktur und Funktion von RNA genau vorhersagen und spielt eine wichtige Rolle bei der Verbesserung der Entwicklung von RNA-Therapien Papierlink: https://doi.org/10.1101/2023.12.13.571579
Dr. Manjunath Ramarao, wissenschaftlicher Leiter von Atomic AI, sagte: 
Das erste RNA-basierte Modell, das auf chemischen Kartendaten trainiert wurde
Um diese Designherausforderung anzugehen, hat Atomic AI ATOM-1 auf den Markt gebracht, das erste RNA-basierte Modell, das auf chemischen Kartendaten trainiert wurde, und zwar mithilfe einer Datenerfassungsstrategie, die speziell für das Training des maschinellen Lernens entwickelt wurde. Mithilfe eines kleinen neuronalen Sondennetzwerks auf ATOM-1-Einbettungen zeigen wir, dass dieses Modell eine reichhaltige interne Darstellung der RNA entwickelt hat. Diese kleinen Netzwerke wurden mit einer begrenzten Menge zusätzlicher Daten trainiert und erzielten bei wichtigen RNA-Vorhersageaufgaben höchste Genauigkeit. Dies zeigt, dass dieser Ansatz therapeutisches Design im gesamten RNA-Bereich ermöglichen könnte.
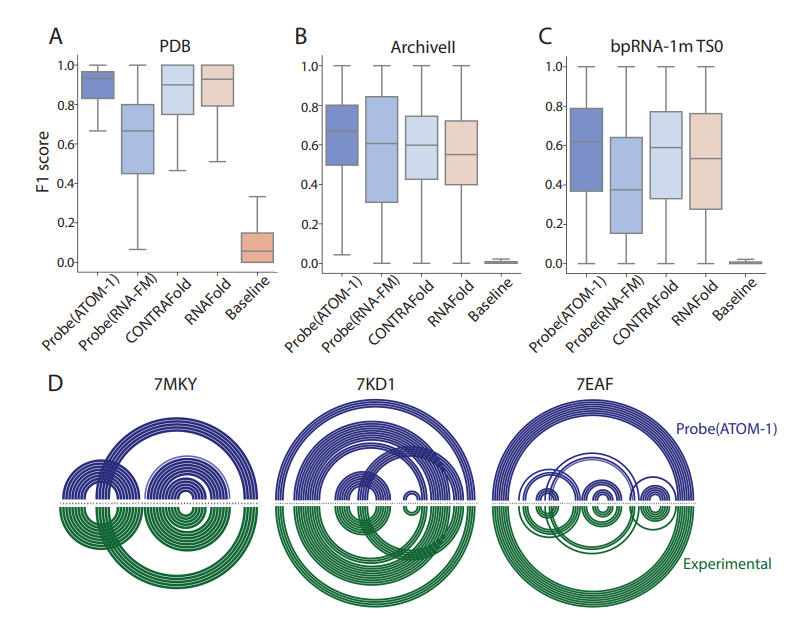
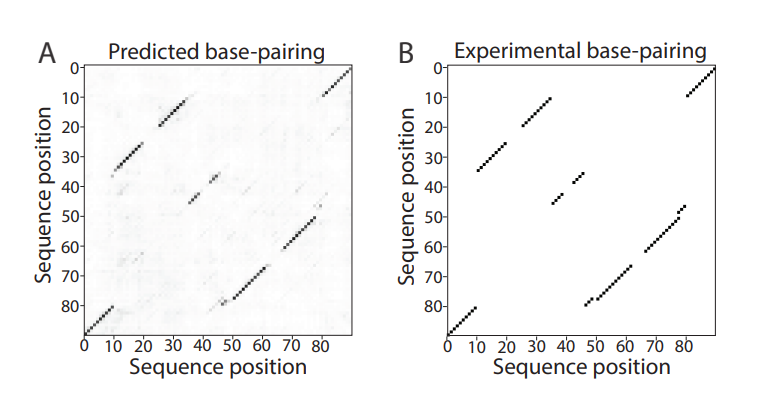
ATOM-1 kann die Sekundär- und Tertiärstrukturen von RNA genauer vorhersagen als zuvor veröffentlichte Methoden
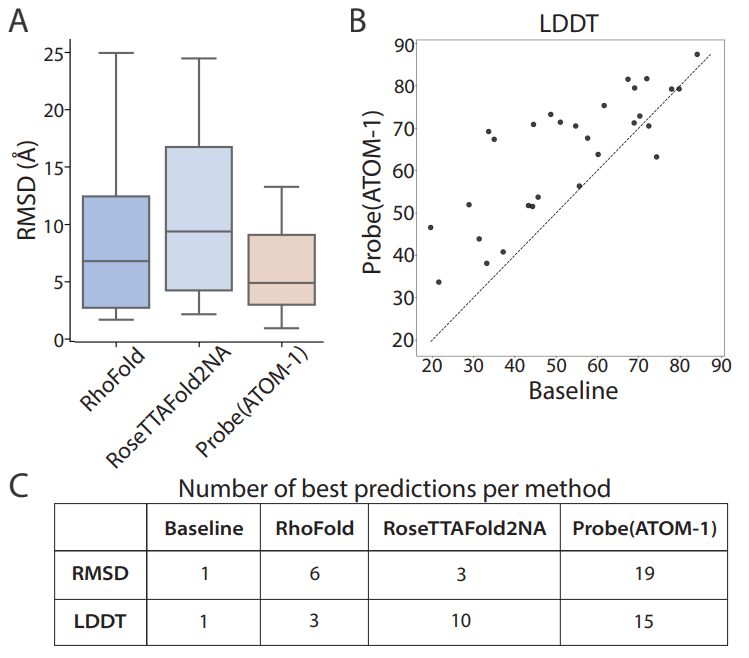
Bemerkenswert ist, dass ATOM-1 in einer retrospektiven Analyse, in der ATOM-1 mit anderen Computertools für die Impfstoffentwicklung verglichen wurde, alle 1.600 anderen Methoden zur Vorhersage der mRNA-Stabilität in Lösung übertraf. Basierend auf diesen Ergebnissen können neue zugrunde liegende Modelle mit begrenzten Daten angepasst werden, um verschiedene Eigenschaften von RNA vorherzusagen und nicht nur die Struktur von RNA zu bestimmen, sondern auch andere Schlüsselmerkmale von RNA-Therapeutika vorherzusagen.
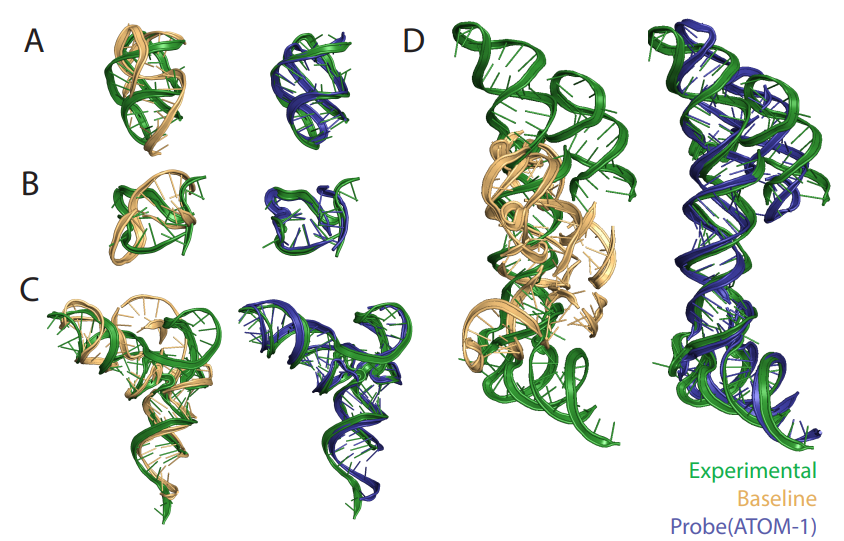
Seit zweieinhalb Jahren haben wir gezielt Daten entworfen und gesammelt, um unser Basismodell zu trainieren, sagte Dr. Raphael Townshend, Gründer und CEO von „Atomic AI“. „Durch maschinelles Lernen und generative künstliche Intelligenz haben wir jetzt die einzigartige Möglichkeit, ATOM-1 mit einer kleinen Anzahl anfänglicher Datenpunkte so abzustimmen, dass die RNA-Struktur und -Funktion mit hoher Genauigkeit vorhergesagt werden kann.“
Zeng erschien auf dem Cover von Science, Atomic AIs proprietäre KI-gesteuerte 3D-RNA-Struktur-Engine
Atomic AI ist ein aufstrebendes Biotechnologieunternehmen, das im Mai 2021 gegründet wurde und seinen Hauptsitz in der San Francisco Bay Area hat. Das Unternehmen konzentriert sich darauf, die Kombination von maschinellem Lernen und Strukturbiologie zu nutzen, um die Entdeckung von RNA-Arzneimitteln voranzutreiben. Sie haben eine proprietäre Plattform entwickelt, die Deep-Learning-Grundmodelle verwendet, um kleine Moleküle, die auf RNA abzielen, RNA-basierte Medikamente und RNA-Werkzeuge zu erforschen und zu entwerfen of RNA Structure“ „Deep Learning of RNA Structure“) ist auf dem Cover des Science-Magazins erschienen.
 Link zum Science-Titelartikel: https://www.science.org/doi/10.1126/science.abe5650
Link zum Science-Titelartikel: https://www.science.org/doi/10.1126/science.abe5650
Seine bahnbrechende Technologie sagt strukturierte, ligandierbare Liganden mit beispielloser Geschwindigkeit und Genauigkeit von RNA-Motiven voraus. Dies ist ein Haupthindernis bei aktuellen Methoden zur RNA-Wirkstoffentdeckung.
Durch die Kombination fortschrittlicher Algorithmen und groß angelegter experimenteller Biologieforschung können neuartige RNA-gerichtete Medikamente und RNA-basierte Medikamente entwickelt werden, um Krankheiten zu behandeln, für die es derzeit keine vermarkteten Medikamente gibt.
Durch die Nutzung der 3D-RNA entdecken und entwerfen wir Structural Datenbank plant Atomic AI, die Entwicklung einer Reihe rational gestalteter Arzneimittelkandidaten mit kleinen Molekülen voranzutreiben
Atomic AI hat in zwei Investitionsrunden insgesamt 42 Millionen US-Dollar eingesammelt, die letzte davon war eine Serie-A-Finanzierung im Januar 2023. Atomic AI hat in zwei Investitionsrunden insgesamt 42 Millionen US-Dollar an Finanzmitteln eingeworben, die letzte davon war eine Finanzierung der Serie A im Januar 2023.
Atomic AI ist führend auf dem Gebiet der durch künstliche Intelligenz verbesserten Strukturbiologie, angetrieben durch Maschinen Team aus Lernforschern, medizinischen Chemikern, Ingenieuren und Experimentalbiologen sowie strategischen wissenschaftlichen Beratern und erstklassigen Investoren. Durch die Änderung des Designs von RNA-Medikamenten konnten sie unbehandelbare Krankheiten erfolgreich behandeln /
Das obige ist der detaillierte Inhalt vonDurchbruch in der RNA-Arzneimittelentwicklung: Das erste RNA-Basismodell enthüllt Messtechnik auf der Ebene von mehr als einer Milliarde Nukleotiden. Für weitere Informationen folgen Sie bitte anderen verwandten Artikeln auf der PHP chinesischen Website!

